Bộ Y tế: Thu hồi giấy đăng ký lưu hành 3 loại thuốc theo đề nghị tự nguyện
Cụ thể, 3 loại thuốc bị thu hồi giấy đăng ký lưu hành do chính cơ sở đăng ký thuốc đề nghị tự nguyện ngừng lưu hành các sản phẩm này tại thị trường Việt Nam. Các thuốc bị thu hồi gồm:
1. Tadalafil 20mg. Số đăng ký: 893110457024 (SĐK cũ: VD-31364-18). Cơ sở đăng ký và sản xuất: Công ty Liên doanh Meyer-BPC. Địa chỉ: 6A3, Quốc lộ 60, phường Phú Tân, thành phố Bến Tre, tỉnh Bến Tre.
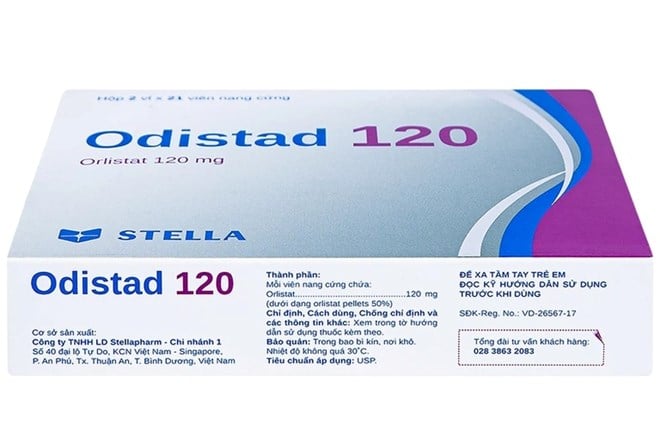
Thu hồi thuốc Odistad 120 theo đề nghị tự nguyện của các cơ sở đăng ký (Ảnh: Long Châu)
2. Odistad 120. Số đăng ký: 893100515124 (SĐK cũ: VD-21535-14). Cơ sở đăng ký: Công ty TNHH Liên Doanh Stellapharm. Địa chỉ đăng ký: K63/1 Nguyễn Thị Sóc, ấp Mỹ Hòa 2, xã Xuân Thới Đông, huyện Hóc Môn, TP. HCM. Cơ sở sản xuất: Stellapharm - Chi nhánh 1, số 40 Đại lộ Tự Do, KCN VSIP, phường An Phú, TP. Thuận An, tỉnh Bình Dương.
3. Vacobufen 400. Cơ sở đăng ký và sản xuất: Công ty Cổ phần Dược Vacopharm. Địa chỉ đăng ký: 59 Nguyễn Huệ, phường 1, TP. Tân An, tỉnh Long An. Địa chỉ sản xuất: Km 1954, Quốc lộ 1A, phường Tân Khánh, TP. Tân An, tỉnh Long An.
Theo đó, các thuốc đã được sản xuất trước thời điểm quyết định có hiệu lực vẫn được phép tiếp tục lưu hành cho đến khi hết hạn sử dụng. Tuy nhiên, các cơ sở đăng ký và sản xuất thuốc vẫn phải chịu hoàn toàn trách nhiệm trong việc theo dõi chất lượng, đảm bảo an toàn và hiệu quả của thuốc trong suốt quá trình lưu hành còn lại.
Đồng thời, Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, các cơ sở kinh doanh dược, cũng như giám đốc các cơ sở đăng ký và sản xuất các loại thuốc nêu trên phải nghiêm túc thực hiện nội dung trong quyết định.
Đăng Khải
- Sản phẩm vì sức khỏe
-
Xác thực truy xuất nguồn gốc - 'thuốc đặc trị' chống hàng giả
Khi nền kinh tế số đang trở thành một trong những trụ cột phát triển của đất nước, thì yêu cầu về tính xác thực, minh bạch và khả năng truy xuất nguồn gốc của hàng hóa không chỉ phục vụ công tác quản lý nhà nước mà còn là điều kiện tiên quyết để nâng cao niềm tin thị trường trong nước và hội nhập quốc tế.July 9 at 8:25 am -
Công tác đánh giá, phân hạng sản phẩm OCOP được chia thành 02 cấp
Phó Thủ tướng Trần Hồng Hà ký Quyết định số 1489/QĐ-TTg ngày 6/7/2025 sửa đổi, bổ sung một số nội dung Quyết định số 148/QĐ-TTg về việc phê duyệt Bộ tiêu chí và quy trình đánh giá, phân hạng sản phẩm Chương trình mỗi xã một sản phẩm (OCOP).July 7 at 7:32 am -
Lấy lại nụ cười tự tin với dịch vụ bọc răng sứ tại TCI
Hàng nghìn khách hàng đã tìm lại nụ cười tự tin nhờ dịch vụ bọc răng sứ tại Khoa Răng Hàm Mặt bệnh viện Đa khoa Quốc tế (ĐKQT) Thu Cúc TCI.July 3 at 12:01 pm -
Đau họng, ợ hơi, tức ngực: Người đàn ông ngỡ ngàng phát hiện ung thư đại tràng sớm qua nội soi
Người đàn ông 37 tuổi khỏe mạnh bàng hoàng phát hiện có tổn thương nguy cơ ung thư nhờ công nghệ nội soi hiện đại tại Bệnh viện Thu Cúc. Câu chuyện của anh là hồi chuông cảnh tỉnh cho nhiều người trẻ còn đang chủ quan, thờ ơ với sức khỏe tiêu hóa.July 2 at 10:13 am




 Từ khóa:
Từ khóa: