Đình chỉ lưu hành, thu hồi và tiêu hủy mỹ phẩm Dung dịch vệ sinh Yoko Eva Collagen của Công ty Dược phẩm Yoko Pharma
Căn cứ Điều 70 Nghị định số 117/2020/NĐ-CP ngày 28/9/2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế;
Căn cứ Điều 2 Nghị định số 124/2021/NĐ-CP ngày 28/12/2021 của Chính phủ sửa đổi, bổ sung một số điều của Nghị định số 115/2018/NĐ-CP ngày 04/9/2018 của Chính phủ quy định xử phạt vi phạm hành chính về an toàn thực phẩm và Nghị định số 117/2020/NĐ-CP ngày 28/9/2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế;

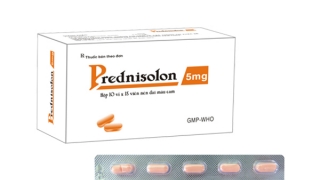
(Ảnh minh họa)
Căn cứ Điều 45, Điều 46 Thông tư số 06/2011/TT-BYT ngày 25/01/2011 của Bộ Y tế quy định về quản lý mỹ phẩm; Căn cứ Công văn số 234/SYT-NVD đề ngày 21/10/2024 của Sở Y tế tỉnh Hưng Yên gửi kèm Công văn số 149/TTKN ngày 08/10/2024 của Trung tâm kiểm nghiệm thuốc, mỹ phẩm, thực phẩm - Sở Y tế Hưng Yên, Phiếu kiểm nghiệm số 478 ngày 26/8/2024 và hồ sơ liên quan báo cáo lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml, trên nhãn ghi Số lô: 060722; NSX: 02/07/22; HSD: 01/07/25; Số công bố: 12702/22/CBMP-HN; Tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH dược phẩm Yoko Pharma (Địa chỉ: Tổ dân phố Phan, phường Bạch Sam, thị xã Mỹ Hào, tỉnh Hưng Yên); Công ty cổ phần dược phẩm công nghệ Bibita (Địa chỉ: Thôn Nghĩa Hảo, xã Phú Nghĩa, huyện Chương Mỹ, TP. Hà Nội) sản xuất.
Mẫu mỹ phẩm trên do Trung tâm Kiểm nghiệm thuốc, mỹ phẩm, thực phẩm - Sở tỉnh Hưng Yên lấy mẫu tại Quầy thuốc Bạch Mai (Địa chỉ: 723 Nguyễn Thiện Thuật, phường Phan Đình Phùng, thị xã Mỹ Hào, tỉnh Hưng Yên) để kiểm tra chất lượng. Mẫu thử không đạt tiêu chuẩn chất lượng về chỉ tiêu độ pH.
Cục Quản lý Dược thông báo:


1. Đình chỉ lưu hành, thu hồi trên toàn quốc lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml, trên nhãn ghi Số lô: 060722; NSX: 02/07/22; HSD: 01/07/25; Số công bố: 12702/22/CBMP-HN; Tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường: Công ty TNHH dược phẩm Yoko Pharma (Địa chỉ: Tổ dân phố Phan, phường Bạch Sam, thị xã Mỹ Hào, tỉnh Hưng Yên); Công ty cổ phần dược phẩm công nghệ Bibita (Địa chỉ: Thôn Nghĩa Hảo, xã Phú Nghĩa, huyện Chương Mỹ, TP. Hà Nội) sản xuất. Lý do thu hồi: Mẫu kiểm nghiệm không đạt tiêu chuẩn chất lượng về chỉ tiêu độ pH và mỹ phẩm lưu thông có nhãn lưu hành ghi sai lệch bản chất tính năng vốn có của sản phẩm.
2. Đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương:
- Thông báo cho các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml nêu trên và trả lại cơ sở cung ứng sản phẩm;
- Tiến hành thu hồi và tiêu hủy lô sản phẩm vi phạm nêu trên; kiểm tra, giám sát các đơn vị thực hiện thông báo này; xử lý các đơn vị vi phạm theo quy định hiện hành.
3. Công ty TNHH dược phẩm Yoko Pharma, Công ty cổ phần dược phẩm công nghệ Bibita phải:
- Gửi thông báo thu hồi tới những nơi phân phối, sử dụng lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml nêu trên; Tiếp nhận sản phẩm trả lại từ các cơ sở kinh doanh và tiến hành thu hồi, tiêu hủy toàn bộ sản phẩm không đáp ứng quy định.
- Gửi báo cáo thu hồi và tiêu hủy lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml nêu trên về Cục Quản lý Dược trước ngày 16/12/2024.
4. Đề nghị Sở Y tế TP. Hà Nội, Sở Y tế tỉnh Hưng Yên:
- Giám sát Công ty TNHH dược phẩm Yoko Pharma, Công ty cổ phần dược phẩm công nghệ Bibita trong việc thực hiện thu hồi và tiêu hủy lô sản phẩm Dung dịch vệ sinh Yoko Eva Collagen - Hộp 1 lọ 100 ml không đáp ứng quy định.
- Kiểm tra Công ty TNHH dược phẩm Yoko Pharma, Công ty cổ phần dược phẩm công nghệ Bibita trong việc chấp hành các quy định của pháp luật về quản lý mỹ phẩm trong hoạt động sản xuất, kinh doanh mỹ phẩm; Xử lý, xử phạt vi phạm theo quy định hiện hành.
- Báo cáo kết quả kiểm tra, giám sát về Cục Quản lý Dược trước ngày 31/12/2024. Cục Quản lý Dược thông báo để các Sở Y tế, Công ty biết và triển khai thực hiện.
Thu Hằng
- Sản phẩm vì sức khỏe
-
Công tác đánh giá, phân hạng sản phẩm OCOP được chia thành 02 cấp
Phó Thủ tướng Trần Hồng Hà ký Quyết định số 1489/QĐ-TTg ngày 6/7/2025 sửa đổi, bổ sung một số nội dung Quyết định số 148/QĐ-TTg về việc phê duyệt Bộ tiêu chí và quy trình đánh giá, phân hạng sản phẩm Chương trình mỗi xã một sản phẩm (OCOP).July 7 at 7:32 am -
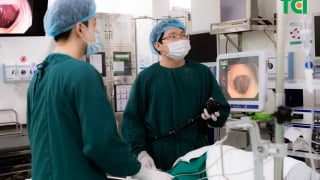
Đau họng, ợ hơi, tức ngực: Người đàn ông ngỡ ngàng phát hiện ung thư đại tràng sớm qua nội soi
Người đàn ông 37 tuổi khỏe mạnh bàng hoàng phát hiện có tổn thương nguy cơ ung thư nhờ công nghệ nội soi hiện đại tại Bệnh viện Thu Cúc. Câu chuyện của anh là hồi chuông cảnh tỉnh cho nhiều người trẻ còn đang chủ quan, thờ ơ với sức khỏe tiêu hóa.July 2 at 10:13 am -
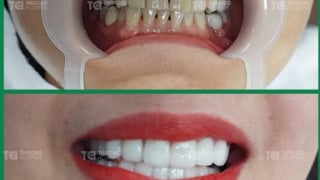
Lấy lại nụ cười tự tin với dịch vụ bọc răng sứ tại TCI
Hàng nghìn khách hàng đã tìm lại nụ cười tự tin nhờ dịch vụ bọc răng sứ tại Khoa Răng Hàm Mặt bệnh viện Đa khoa Quốc tế (ĐKQT) Thu Cúc TCI.July 1 at 12:01 pm -
Chấm dứt ợ hơi, ợ chua, mất ngủ nhờ phương pháp đo áp lực thực quản HRM hiện đại
Từng khổ sở với ợ hơi, ợ chua, nuốt vướng và mất ngủ triền miên, chị H.T.B.L (38 tuổi) đã tìm lại giấc ngủ ngon và sức khỏe chỉ sau thời gian ngắn điều trị tại Bệnh viện Đa khoa Quốc tế Thu Cúc nhờ kỹ thuật đo áp lực và nhu động thực quản độ phân giải cao HRM.July 1 at 12:00 pm




 Từ khóa:
Từ khóa: